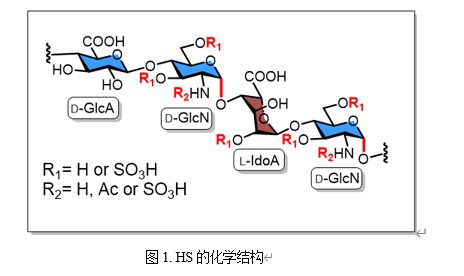
硫酸乙酰肝素(Heparan sulfate, HS)是糖胺聚糖(Glycosaminoglycan, GAG)家族中的重要成员,广泛存在于细胞表面及细胞外基质中。HS在高尔基体中经糖基转移酶催化合成,其结构由D-葡萄糖胺(GlcN)与D-葡萄糖醛酸(GlcA)[GlcN-α-1,4-GlcA-β-1,4-]或D-葡萄糖胺与L-艾杜糖醛酸(IdoA)[GlcN-α-1,4-IdoA-α-1,4-]组成的二糖重复单元构成。该骨架在糖醛酸的C2-OH位,以及葡萄糖胺的C6-OH、C3-OH和C2-NH₂位具有多个硫酸化位点(图1)。这种广泛的硫酸化修饰使HS带有高负电荷,赋予其独特的蛋白质-聚糖相互作用特性,并介导多种生物学功能,然而,该聚糖结构高度复杂且具有显著异质性,这为获取精确结构的该样品并用于后续生物活性的研究带来了巨大的挑战。目前,HS在液相中的化学合成已得到较好发展,并在构建HS化合物库方面取得了许多重要成果。尽管如此,该领域的深入发展仍需在糖化学专业知识的支撑下开展,并投入持续而系统的研究努力。
固相聚糖合成(Solid-phase glycan synthesis, SPGS)是制备结构明确聚糖的一种高效技术,它能显著简化聚糖组装过程中间产物的纯化步骤。自2001年实现自动化聚糖组装(Automated Glycan Assembly, AGA)以来(Science2001,291, 1523-1527),过去二十年间已有多种具有不同生物学功能的聚糖通过该方法成功制备,包括具有反式糖苷键连接的糖胺聚糖,如硫酸软骨素、硫酸皮肤素和硫酸角质素。然而,在固相上构建含多个顺式糖苷键的聚糖仍是一项具有挑战性的工作,因为在链延伸过程中无法分离立体异构体。目前仅有少数关于固相组装含多个顺式糖苷键聚糖的报道。对于HS,由于葡萄糖胺和糖醛酸结构单元的反应活性较低,其固相合成面临更大挑战,需要同时解决反应活性与立体选择性问题。
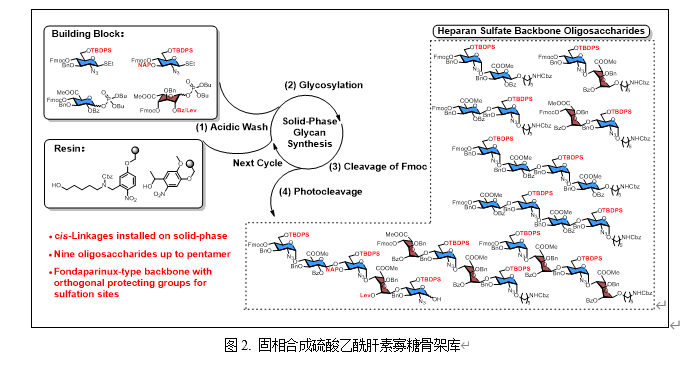
近日,2138cc太阳集团朱蕴韬教授课题组在中科院一区期刊Chinese Journal of Chemistry上发表了题为“Synthesis of Heparan Sulfate Backbone Oligosaccharides by Directly Installing cis-Linkages on Solid-Phase”的研究工作。本研究成功制备了一个包含九种硫酸乙酰肝素骨架寡糖的化合物库,其中GlcN、GlcA和IdoA之间的顺式糖苷键均在固相中构建(图2)。作者首先在液相中对十种具有不同C3-OH和C6-OH保护基组合的2-叠氮-2-脱氧硫代吡喃葡萄糖苷进行了糖基化条件探索。该研究发现,C6-OH位含有TBDPS保护基的硫代吡喃葡萄糖苷在构建GlcN与GlcA/ IdoA之间的α-1,4糖苷键时为最适供体。此外,根据团队先前的研究,在具有C2-OBn的葡萄糖硫苷进行糖基化时,3,6-位酯化可显著促进顺式选择性(J. Am. Chem. Soc.2021,143, 9758–9768)。本研究中砌块9和10 (图3)的结果进一步证实了这一结论。
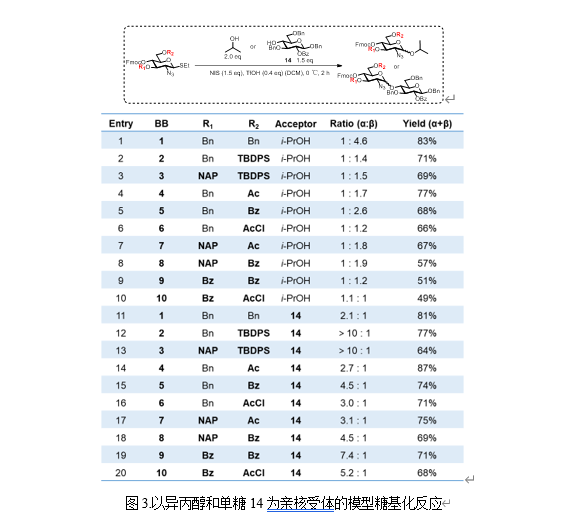
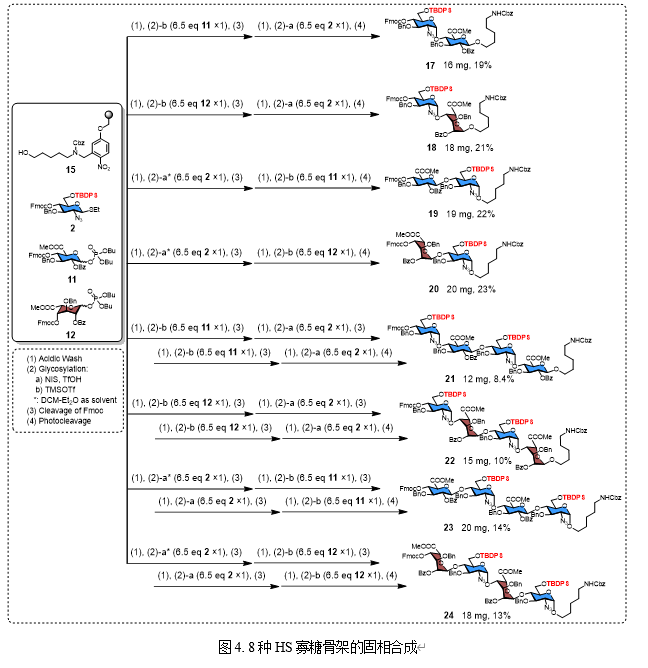
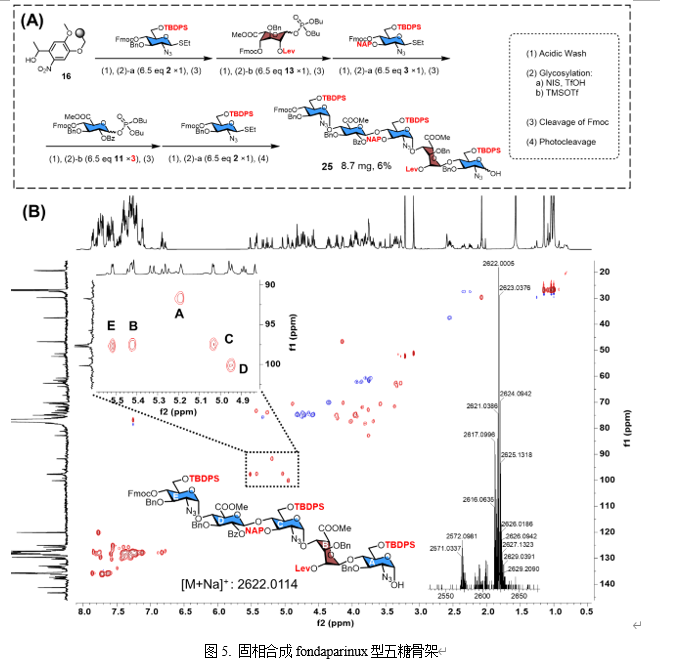
在固相构建HS寡糖骨架初期,作者测试了带有碱敏感连接子的Merrifield树脂(Chem. Eur. J.2025,31, e202500603),但由于碱切过程不仅会切断寡糖与树脂的连接并脱除Bz保护基,还会同时裂解TBDPS保护基并部分水解羧酸甲酯,导致其不适用于在潜在硫酸化位点引入正交保护基,因此该方案被放弃。作者最终选用含有光裂解连接子的固相载体进行后续研究,并在固相上成功合成了四个由GlcN-GlcA或GlcN-IdoA交替重复组成的二糖和四个四糖(图4)。最后,作者合成了一种包含GlcN、GlcA和IdoA结构单元的fondaparinux型五糖(图5)。所有潜在硫酸化位点均通过正交保护策略实现,获得了可接受的产率与优异的α-立体选择性,首次在固相上实现同时含有GlcN、GlcA和IdoA结构单元的完整HS骨架寡糖合成。该策略无需借助预制二糖砌块,而是在固相体系中原位构建了具有合成挑战性的顺式糖苷键,为复杂肝素寡糖化合物库的自动化构建提供了研究基础与有价值参考。
2138cc太阳集团硕士研究生王双丽为本文第一作者,朱蕴韬教授与助理研究员朱攀博士为共同通讯作者。工作得到了国家自然科学基金委、教育部、江苏省教育厅及2138cc太阳集团相关项目经费的支持。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/cjoc.70473